斐林试剂

斐林試劑中的活化劑——二酒石酸根合铜(II)離子的球棒模型
斐林试剂(Fehling's reagent),也称斐林试液、菲林试剂,是一个常用的分析化学试剂。西元1849年由德國化學家赫爾曼·馮·斐林制作出來。斐林試劑可以用來區分水溶性的醛及酮官能基,也可以用來測定單醣。[1]
目录
1 製備
2 总反应式
3 安全性
4 参见
5 参考资料
6 外部連結
製備
通常在需要使用斐林試劑時,會直接在實驗室調配。它由兩個試劑混合制得,分別是斐林試液A和斐林試液B。斐林試液A為藍色硫酸銅水溶液,斐林試液B為酒石酸鉀鈉(或稱羅謝爾鹽)和強鹼氫氧化鈉的无色透明混合溶液。兩種試液配製方法如下:
- 斐林试液A:由69.28g的五水合硫酸铜溶于1L蒸馏水中得到;
- 斐林试液B:由346g的四水合酒石酸钾钠和120g氢氧化钠溶于1L蒸馏水中得到。
將以上兩試液等體積混合即可得到深藍色的斐林試劑。斐林試劑中由酒石酸鉀鈉解離出來的酒石酸根離子(C4H4O62-)与銅離子(Cu2+(aq))螯合形成雙齒配合物二酒石酸根合铜(II)離子(如下圖所示),从而防止溶液中的硫酸銅和氫氧化鈉反應形成氫氧化銅(CuSO4+NaOH→Cu(OH)2)。
斐林試劑可以用于鉴定含有羰基的化合物是否為醛或酮。試劑中的二價雙酒石酸鹽負離子螯合物為氧化劑和此檢測中的活化劑。將待測試的物質加入斐林試劑中混合並共熱,若化合物中具有醛基則會被氧化呈陽性反應,此外除具有α-羥基酮官能基的化合物,其他酮類皆不與斐林試劑反應。
该反應原理是二價雙酒石酸鹽負離子會去氧化羧酸陽離子,在這個過程中螯合物的中央二價銅離子被還原成為一價銅離子(即發生了氧化還原反應),形成磚紅色的氧化亞銅沉澱,此即斐林試劑的陽性反應結果(同為本尼迪克試劑的陽性反應)。反之,沒有發生沉澱則為陰性結果;若待測試物質為芳香醛類則不會與斐林試劑反應,而應使用吐倫試劑進行檢測。
斐林試劑因可与醛糖反應(具有醛基)而常用于檢驗是否存在單醣。另外特別的是酮糖也可以用此法檢測,这是由于酮糖类的单糖(如果糖)會与斐林试剂中的鹼作用,使之转化为醛糖,进而可以被斐林试剂氧化从而呈陽性反应。[2] 因此斐林試劑常用于單醣的檢測。
斐林試劑也可以用于檢測糖尿病,它可以與尿中的葡萄糖反應。還有另一個用途是把澱粉分解成葡萄糖漿和麥芽糊精(maltodextrin)以測定還原糖的量,也就是所謂的葡萄糖當量(Dextrose equivalent,DE)。
甲酸(HCOOH)在斐林測試中呈陽性反應,在與吐倫試劑和本尼迪克試劑的測試中也同樣會呈陽性反應,這是因為其易被氧化成二氧化碳和水。
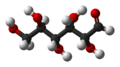
葡萄糖的醛式結構

[CuII(酒石酸根)2]4− 配离子

氧化亚铜的晶体结构
斐林測試,左試管呈陰性反應,右試管呈陽性反應
总反应式
醛基与 Cu2+ 在斐林试剂中的总反应可被写为:
RCHO+2Cu2++5OH−⟶RCOO−+Cu2O+3H2O{displaystyle {ce {RCHO + 2 Cu^2+ + 5 OH- -> RCOO- + Cu2O + 3 H2O}}}
加入酒石酸可写为:
RCHO+2Cu(C4H4O6)22−+5OH−⟶RCOO−+Cu2O+4C4H4O62−+3H2O{displaystyle {ce {RCHO{}+ 2 Cu(C4H4O6)_2^{2-}{}+ 5 OH^- -> RCOO^{-}{}+ Cu2O{}+ 4 C4H4O6^{2-}{}+ 3 H2O}}}
安全性
試劑中之氫氧化鈉具有腐蝕性,所以應注意不要跟皮膚接觸。另外硫酸銅屬於重金屬鹽,若誤食會造成中毒,成人致死劑量0.9g/kg。[2]
参见
銀氨溶液(多倫試劑)- 本尼迪克试剂
参考资料
^ H. Fehling. Die quantitative Bestimmung von Zucker und Stärkmehl mittelst Kupfervitriol. Annalen der Chemie und Pharmacie. 1849, 72 (1): 106–113. doi:10.1002/jlac.18490720112.
^ 2.02.1 Fehling's Test for Reducing Sugars
外部連結
- [1]






